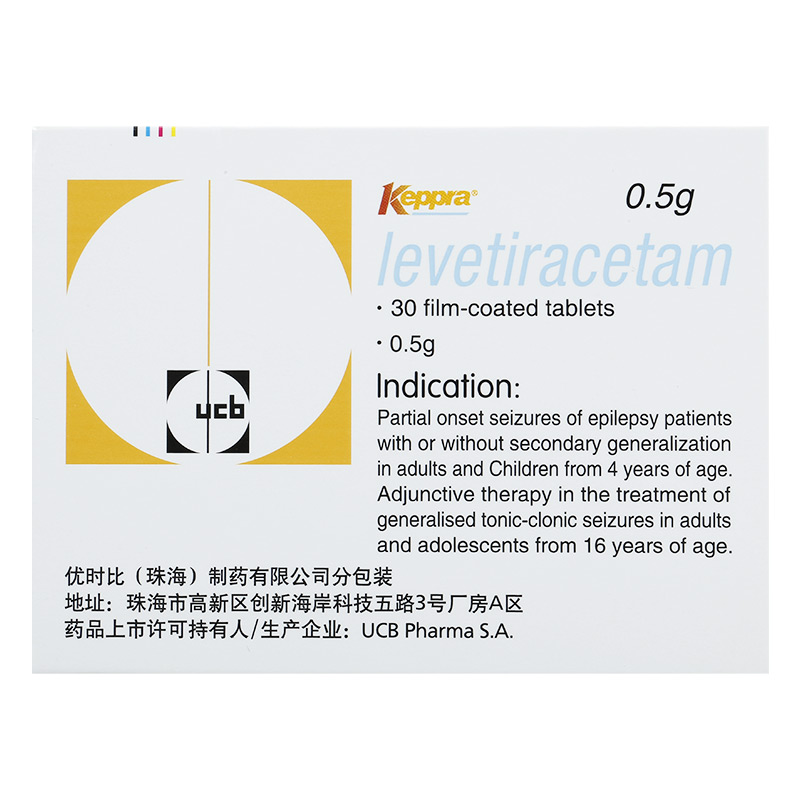
主要成份
本品的活性成份为左乙拉西坦,其化学名称为(S)-a-乙基-2-氧代-1-吡咯烷乙酰胺
功能主治
用于成人及4岁以上儿童癲痛患者部分性发作(伴或不伴继发性全面性发作)的治疗。 用于成人及16岁以上青少年癫痛患者全面性强直阵孪发作的加用治疗。
用法用量
(1) 给药途径: 口服。需以适量的水吞服,服用不受进食影响。
(2) 给药方法和剂量
成人(18岁)和青少年(12岁~17岁)体重50kg 起始治疗剂量为每次500mg,每日 2次。根据临床效果及耐受性,每日剂量可增加至每次1500mg,每日两次。剂量的变化应每2-4周增加或减少500mg/次, 每日2次。
老年人 (65岁)根据肾功能状况,调整剂量 (详见下文有关肾功能受损病人描述)。
4~11岁的儿童和青少年(12-17岁)体重50kg起始治疗剂量是10mg/kg,每日两次。根据临床效果及耐受性,剂量可以增加至30mg/kg, 每日两次。 剂量变化应以每两周增加或减少10mg/kg,每日两次。应尽量使用最低有效剂量。儿童和青少年体重50kg,剂量和成人一致。
青少年和儿童推荐剂量
体重 起始剂量:10mg/kg,每日两次 最大剂量:30mg/kg,每日两次
15kg 每次150mg,每日两次 每次450mg,每日两次
20kg 每次200mg,每日两次 每次600mg,每日两次
25kg 每次250mg,每日两次 每次750mg,每日两次
50kg起 每次500mg,每日两次 每次1500mg,每日两次
20kg 以下的儿童,为精确调整剂量,起始治疗应使用口服溶液。
婴儿和小于4岁的儿童患者目前尚无相关的充足的资料。
肾功能受损的病人 成人肾功能受损病人,根据肾功能状况,按表中不同肌苷清除率(CLcr)ml/min(测出血清肌苷值按下述计算方法)调整日剂量.。
CLcr=[140-年龄(岁)]*体重(公斤) / [72*血清肌酐值(mg/dl)]
女性病人*0.85
肾功能受损病人的剂量
病人组 肌酐清除率(ml/min) 剂量和服用次数
正常病人 80 每次500-1500mg,每日两次
轻度异常 50-79 每次500-1500mg,每日两次
中度异常 30-49 每次250-750mg,每日两次
严重异常 [30 每次250-500mg,每日两次
正在进行透析晚期肾病病人(1)-- 500-1000mg,每日一次(2)
(1)服用第一天推荐负荷剂量为左乙拉西坦750mg。(2)透析后,推荐给予250-500mg附加剂量。儿童肾功能损害病人应根据肾功能状态调整剂量,因为左乙拉西坦的清除与肾功能有关。肝病患者对于轻度和中度肾功能受损的病人,无需调整给药剂量。严重肝损的病人,肌酐清除率可能低估肾功能不全的程度,因此,如果病人的肌酐清除率小于70ml/min,日剂量减半。
药品相互作用
体外数据显示:治疗剂量范围内获得的高于Cmax水平的浓度时左乙拉西坦及其主要代谢物,既不是人体肝脏细胞色素P450、环氧化水解酶或尿苷二磷酸葡萄苷酶的抑制剂,也不是它们具有高亲合力的底物。因此,不易出现药代动力学相互作用。另外,左乙拉西坦不影响丙戊酸的体外葡萄苷酶作用。左乙拉西坦血浆蛋白结合率低(<10%) ,不易产生因与其他药物竞争蛋白结合位点所致临床显著性的相互作用。临床药代动力学研究(苯妥英、丙戊酸钠、口服避孕药、地高辛、华法令和丙磺舒)和安慰剂对照临床试验中通过药代动力学筛选评估了药物之间的潜在药代动力学相互作用。左乙拉西坦和其他抗癫痈药物(AEDs) 间的药物-药物相互作用苯妥英左乙拉西坦(每日3000mg) 对难治性的癫痛病人苯安英药代动力学特性不产生作用。苯妥英的应用也不影响本品的药代动力学特性。丙戊酸钠左乙拉西坦( 1500mg每日2次)不改变健康志愿者丙戊酸钠药代动力学特性。丙戊酸钠500mg每日2次,不改变左乙拉西坦吸收的速率或程度,或其血浆清除率,或尿液排泄。也不影响主要代谢产物ucbL057的暴露水平和排泄。对安慰剂对照临床研究获得的左乙拉西坦和其他抗癫痛药物(卡马西平、加巴喷丁、拉莫三嗪、苯巴比妥、苯妥英、去氧苯巴比安和丙戊酸钠)的血清浓度进行了评估,数据显示左乙拉西坦不影响其他抗癫痛药物的血药浓度。这些常用的抗癫痫药物也不影响本品药代动力学特性。儿童病人抗瘦痛药物的作用同时服用酶诱导型抗癫痛药,本品体内表观总清除率增加约22%。但无需进行剂量调整。左乙拉西坦不影响卡马西平、丙戊酸钠、托吡酯或拉莫三嗪的血浆药物浓度。其他药物相互作用口服避孕药服用左乙拉西坦( 500mg每日2次)不影响含有0.03mg炔雌醇和0.15mg左炔诺孕酮口服避孕药的药代动力学特性,或促黄体激素和黄体酮含量水平,表明本品不影响避孕药功效。应用口服避孕药,并不影响本品的药代学特性。地高辛服用左乙拉西坦( 1000mg每日2次)不影响每日剂量025mg地高辛的药代动力学和药效学(ECG) 特性。应用地高辛,并不影响本品的药代学特性。华法令服用左乙拉西坦( 1000mg每日2次)不影响R和S型华法令的药代动力学特性。凝血时间不受左乙拉西坦影响。应用华法令,并不影响本品的药代学特性。丙磺舒丙磺舒(500mg每日4次),为肾小管分泌阻滞剂,会抑制左乙拉西坦的主要代谢产物的肾脏清除宰但不是左乙拉西坦药代学特性(1000mg,每日2次),但这些代谢物的浓度很低。其他需经肾小管分泌清除的药物也会影响代谢物的肾脏清除。目前无左乙拉西坦合并丙磺舒用药的研究,左乙拉西坦合并应用其他主动分泌药物对药效影响( 例如非甾体抗炎药、磺胺药和甲氨蝶呤),尚不明确。
特殊人群用药
孕妇及哺乳期妇女用药:有生育能力的女性对于有生育能力的女性,应给予专家意见。当一名妇女计 划怀孕时,应评估左乙拉西坦治疗。与所有抗癫痫药一样,应避免突然停用左乙拉西坦,因为这可能导致突发性癫痛发作,可能对孕妇和未出生的胎儿产生严重的后果。在可能的情况下,应首选单药治疗,因为多种抗癫痢药(AED)治疗的先天性畸形风险可能高于单药治疗,这取决于相关抗癫痫药。孕妇大量妊娠妇女暴露于左乙拉西坦单药治疗的上市后数据(超过1800名,其中超过1500名暴露于妊娠早期)未提示重先天畸形风险显著增加。关于宫内暴露于开浦兰单药治疗的儿童出生后其神经发育状况只有有限的证据。然而,目前的流行病学研究(针对大约100名儿童)并未提示神经发有障碍或延迟风险的增加。必须经过仔细评估认为是临床需要后,左乙拉西坦可在怀孕期间使用。在这种情况下,建议使用最低有效剂量。妊娠期间的生理变化会影响左乙拉西坦的浓度。怀孕期间左乙拉西坦浓度降低已有报道。在妊娠晚期,左乙拉西坦浓度的降低更明显(最高降幅为妊娠前基线浓度的60%)。应确保给子服用左乙拉西坦的孕妇适当的临床指导。哺乳左乙拉西坦可以从乳汁中分泌,所以,不建议病人在服药同时哺乳。若在哺乳期间左乙拉西坦治疗是必须的,则需权衡该治疗的获益/风险与哺乳的重要性。生育能力动物研究表明本品对生有能力无影响。但尚无临床研究资料,对人类生育能力的潜在风险不详。儿童用药:见【用法用量】项。老年用药:见【用法用量】项。
注意事项
停药
根据当前的临床实践,如需停止服用本品,建议逐渐停药。(例如:成人和体重50kg或以上的青少年每隔2~4周,每次减少500mg,每日2次:体重< 50kg的儿童和青少年应每隔2周,每次减少10mgkg, 每日2次).
血细胞计数
左乙拉西坦给药后,曾被描述过与之有关的血细胞计数下降(中性粒细胞减少、粒细胞缺乏、白细胞减少、血小板减少和全血细胞减少)。建议出现明显无力、发热、反复感染或凝血障碍的患者接受全血细胞计数的检测。
肾功能不全
对于肾功能损害的患者左乙拉西坦的服用剂量需要调整,对于严重肝功能损害,在选择服用剂量之前,需进行肾功能检测,患者的服用剂量需参照
不良反应
部分性发作的加用治疗
成人临床研究汇总的安全性数据表明,左乙拉西坦组和安慰剂组不良反应的发生率相似,分别为46.4%和42.2%。其中,严重不良反应分别为2.4%和2.0%。最常见的不良反应有嗜睡,乏力和头晕。没有证据表明剂量-反应的关系,随时间的推移,中枢神经系统相关的不良反应发生率和严重程度会随之降低。部分性发作的癫痫儿童患者(4~16岁) 临床研究表明,左乙拉西坦组和安慰剂组产生不良反应的发生率分别为55.4%和40.2%。左乙拉西坦组未发生严重不良反应(安慰剂组1.0%)。儿童最常见的不良反应有嗜睡、敌意、神经质、情绪不稳、易激动、食欲减退、乏力和头痛。汇总分析发现,总的安全性儿童和成人一致,只是行为和精神方面不良反应发生率较成人高(儿童38.6%,成人18.6%),但是儿童发生不良反应的相对风险度与成人相似。1项双盲、安慰剂对照的儿童安全性研究,通过非劣效性设计评估左乙拉西坦对儿童癫痫部分性发作患者(4~16岁)的认知和神经心理学的影响。参考符合方案人群Leiter-R注意及记忆力、记忆筛查综合评分较基线的变化情况,未发现左乙拉西坦和安慰剂之间存在差异(非劣效分析)。应用CBCL-Achenbach儿童行为评定量表对行为情感功能的评估提示,服用左乙拉西坦的患者的攻击行为有所加重。然而,开放性长期随访研究结果显示,服用左乙拉西坦的患者整体上并未出现行为和情感功能的恶化,尤其是攻击行为与基线比较无恶化。全面性强直阵挛发作的加用治疗在中国-日本安慰剂对照研究(16岁及以上)和日本长期随访研究中,安全性分析集的218例成人受试者中出现不良反应的受试者有46例(21.1%)。总体上,最常见的不良反应包括嗜睡(4.6%) 和上呼吸道感染(1.8%) 。除此之外,与异常实验室变化相关的不良反应包括蛋白尿(4.1%)、血小板计数下降(2.3%)和中性粒细胞计数下降(1.8%) 。安全性特征总结总结成人和儿童临床研究结果和上市后经验,评估了每个系统的不良反应和发生频率:非常常见(21/10);常见(21/100,<1/10); 不常见:(21/1000,<1/100); 罕见(21/10000,<1/1000); 非常罕见(<1/10000)。不良反应描述:与托吡酶合用时,厌食的风险较高。一些发生脱发症的患者, 观察到停用左乙拉西坦后有自行恢复的案例。在某些全血细胞减少病例中,观察到骨髓抑制。脑病的不良反应般出现在治疗初期 (几天或者几个月内),是可逆的,停药后可消除。